Alice Dassano*, Maria Elena Lunati**, Antonio Rossi**, Alessandra Gandolfi**, Paolo Fiorina*,**,***
* Centro Internazionale per il T1D, Centro di Ricerca Pediatrica Romeo ed Enrica Invernizzi, “L. Sacco” Dipartimento di Scienze Biomediche e Cliniche, Università degli Studi di Milano, Italia;
** Unità di Endocrinologia e Diabetologia, ASST Fatebenefratelli-Sacco, Milano, Italia;
*** Divisione di Nefrologia, Boston Children’s Hospital, Harvard Medical School, Boston, MA, USA
Grazie al progresso della ricerca scientifica, oggi assistiamo allo sviluppo di approcci innovativi in campo terapeutico che potrebbero in un futuro (forse nemmeno tanto lontano) segnare una svolta nella cura del diabete di tipo 1
Il diabete mellito è una patologia cronica caratterizzata dalla persistenza di elevati livelli di glucosio a livello ematico. Responsabile di questa alterazione è la presenza di deficit relativo o assoluto di insulina, ormone secreto dalle cellule beta nelle isole di Langherhans del pancreas, che consente alle cellule del corpo di internalizzare e utilizzare a livello tissutale il glucosio circolante. Da un punto di vista fisiopatologico, il diabete mellito viene classificato in:
- (i) diabete mellito di tipo 1 (T1D-caratterizzato da deficit assoluto di insulina);
- (ii) diabete mellito di tipo 2 (T2D-causato da un progressivo difetto di secrezione insulinica, associato a un quadro di insulino-resistenza);
- (iii) diabete mellito gestazionale (GDM – diabete diagnosticato durante il periodo gravidico);
- (iv) specifici tipi di diabete relati ad altre cause (diabete monogenico – MODY, diabete neonatale, diabete di tipo 3C, fibrosi cistica, etilismo ecc.) [1].
Inquadramento epidemiologico e clinico
Il T1D, precedentemente definito “diabete insulino-dipendente” o “diabete giovanile”, interessa circa il 5-10 per cento della popolazione diabetica, con una prevalenza in Italia di 1,4 su 1.000 individui e un’incidenza di 10 nuovi casi all’anno su 100.000 persone [2]. T1D è causato dalla distruzione autoimmunitaria delle cellule beta del pancreas [3], mediata da autoanticorpi diretti verso diversi bersagli (tra cui cellule insulari, glutammato-decarbossilasi (GAD65), insulina, tirosin-fosfatasi IA-2 e IA-2b, e ZnT8), nonché da cellule T autoreattive. La velocità di distruzione delle ß-cellule pancreatiche è molto variabile, in alcuni casi estremamente rapida (soprattutto nei bambini e negli adolescenti), in altri casi più lenta (adulti). Sono stati riconosciuti diversi fattori di rischio, tra cui l’appartenenza etnica (soprattutto etnia caucasica e afro-americana), suscettibilità genetica e fattori ambientali, anche se non ancora chiaramente definiti [3].
I pazienti affetti da T1D sono inoltre proni a sviluppare anche altre malattie autoimmuni, come tiroidite di Hashimoto, malattia di Addison, celiachia, vitiligine, epatiti autoimmuni, miastenia grave e anemia perniciosa. Sebbene nella maggior parte dei casi la malattia si sviluppi in individui senza evidente storia familiare di malattia diabetica, i parenti di primo grado di un paziente affetto da T1D hanno un rischio di circa 1 su 20 di sviluppare la malattia, rispetto al rischio di 1 su 300 della popolazione generale [4].
Le manifestazioni cliniche della malattia all’esordio sono variabili. Bambini e adolescenti spesso presentano uno stato di chetoacidosi diabetica (DKA) come prima manifestazione della malattia. DKA è uno stato in cui il deficit insulinico totale determina aumento del catabolismo di acidi grassi e proteine, marcata iperglicemia, alterazioni del pH ematico, squilibrio elettrolitico e comparsa di sintomatologia neurologica, come sonnolenza e letargia. In altri casi, la malattia si manifesta con una moderata iperglicemia che rapidamente evolve in severa iperglicemia e/o DKA in caso di infezioni o altri stress. Soggetti adulti possono avere una funzionalità beta-cellulare residua sufficiente a evitare l’insorgenza di DKA per vari anni. La perdita pressoché totale della secrezione insulinica da parte del pancreas è indicata dalla presenza di livelli estremamente bassi o indosabili di C-peptide, proteina secreta insieme alla molecola di insulina.
Complicanze croniche del diabete
La condizione di iperglicemia prolungata che accompagna l’insorgenza e lo sviluppo del diabete ha effetti indiretti e diretti su vari organi del corpo. Questo determina l’insorgenza di due tipi di complicanze: microvascolari (che includono la retinopatia, la nefropatia e la neuropatia diabetica) e macrovascolari (tra cui troviamo la malattia coronarica, l’arteriopatia periferica e l’ictus). Il rischio di sviluppare queste complicanze dipende sia dalla durata che dalla gravità dell’iperglicemia.
Complicanze microvascolari
Il diabete colpisce l’occhio in molti modi, ma la retinopatia diabetica (DR) è la complicanza oculare più comune e grave. Colpisce un terzo della popolazione diabetica totale, ed è caratterizzata da neovascolarizzazione della retina e compromissione della vista, rappresentando la principale causa di cecità nelle nazioni industrializzate [5]. La nefropatia diabetica è la più comune e invalidante complicanza microvascolare del T1D che colpisce il 30 per cento dei pazienti dopo 25 anni di diabete e aumenta di 37 volte la mortalità cardiovascolare rispetto alla popolazione generale [6]. È generalmente preceduta da una condizione nota come “microalbuminuria”. La microalbuminuria è definita come escrezione di albumina di 30-299 mg in 24 ore. Senza intervento, i pazienti diabetici con microalbuminuria progrediscono tipicamente verso la proteinuria e la nefropatia diabetica conclamata [7].
La neuropatia diabetica si verifica in circa il 34 per cento dei pazienti dopo una media di 15 anni di diabete. È riconosciuta dall’American Diabetes Association (ADA) come “la presenza di sintomi e/o segni di disfunzione dei nervi periferici nelle persone con diabete dopo l’esclusione di altre cause” [8]. Come per le altre complicanze microvascolari, in alcuni individui la predisposizione genetica può avere un ruolo chiave. La natura precisa delle lesioni ai nervi periferici da iperglicemia non è nota, ma probabilmente è correlata a meccanismi quali accumulo di sorbitolo e stress ossidativo, fattori con un possibile ruolo chiave anche nelle altre complicanze associate al diabete [9].
Complicanze macrovascolari
L’arteriopatia periferica e la malattia coronarica rappresentano le principali complicanze cardiovascolari del diabete; la prima ha una mortalità a 5 anni del 30 per cento per ischemia degli arti e la seconda determina un aumento da due a quattro volte del rischio di morte nei soggetti con diabete [10]. Nelle complicanze macrovascolari, il meccanismo patologico centrale è il processo di aterosclerosi, che porta al restringimento delle pareti arteriose. Si ritiene che l’aterosclerosi derivi da infiammazione cronica e danno alla parete arteriosa del sistema vascolare periferico o coronarico che può portare a un infarto vascolare acuto [11]. Sebbene l’associazione tra diabete e arterosclerosi sia ben nota, i precisi meccanismi attraverso i quali il diabete aumenta la probabilità di formazione di placche aterosclerotiche non sono ancora del tutto definiti. La malattia cardiovascolare è la principale causa di morte nelle persone affette da diabete di tipo 1, e rappresenta la componente più importante delle spese sanitarie nelle persone con diabete [12]. Studi recenti hanno dimostrato che il rischio di infarto miocardico (MI) nelle persone con diabete è equivalente al rischio nei pazienti non diabetici con una storia precedente di MI [13].
Queste scoperte hanno portato a nuove raccomandazioni da parte dell’ADA e dell’American Heart Association per considerare il diabete come un equivalente di rischio di malattia coronarica piuttosto che come un fattore di rischio [14]. Il diabete è anche un fattore predittivo di rischio di ictus e malattia cerebrovascolare. Studi hanno dimostrato che pazienti affetti da diabete di tipo 1 hanno una mortalità più elevata dovuta a cardiopatia ischemica a tutte le età rispetto alla popolazione generale. Le donne con età superiore ai 40 anni presentano una mortalità più elevata da cardiopatia ischemica rispetto agli uomini della stessa età [12, 15].
Appartenente sia alle complicanze macrovascolari che a quelle microvascolari c’è infine la complicanza nota come “piede diabetico”. Il piede diabetico è caratterizzato da lesioni ulcerative che insorgono sulla cute del piede in circa il 15 per cento dei pazienti diabetici [16]. È una complicanza che impatta per il 24,4 per cento la spesa sanitaria totale [17]. I meccanismi che ne determinano l’insorgenza sono legati sia alla neuropatia diabetica (precedentemente descritta tra le complicanze microvascolari), che porta alla mancanza di sensibilità a livello del piede e crea un’alterazione anatomica che favorisce la formazione di aree di sovraccarico più facilmente ulcerabili; sia all’arteriopatia periferica (precedentemente descritta tra le complicanze macrovascolari), che determina la mancanza di perfusione distale nel piede determinando l’insorgenza di ulcere ischemiche e, nei casi più gravi, l’amputazione [18].
Terapia insulinica
La terapia insulinica a oggi rimane una pietra miliare del trattamento della patologia diabetica [19]. Nelle ultime decadi, lo sviluppo delle tecniche farmaceutiche ha permesso di ottenere molecole sempre più efficaci e sicure, formulando insuline a breve durata di azione (“analoghi ultra-rapidi”), a lunga durata di azione (“insuline basali” o “analoghi long-acting”) e, infine, insuline a durata di azione intermedia. Le modificazioni farmacocinetiche e farmacodinamiche hanno permesso di ottenere insuline con profilo di azione piatto durante la giornata, migliore riproducibilità giorno per giorno, ridotto rischio di ipoglicemie notturne e durata di azione più prolungata [20]. L’insulina basale, iniettata in tarda serata, sopprime la produzione epatica notturna di glucosio e assicura migliori valori glicemici pre-prandiali mattutini tra cui il controllo del fenomeno dell’alba [21].
Capostipite delle insuline a lunga durata di azione è insulina Glargine U100, ottenuta dalla sostituzione dell’asparagina con la glicina nella posizione 21 della catena A e aggiunta di due arginine nell’estremità terminale C della catena B e caratterizzata da una durata di azione di 20-26 h. Recentemente, due nuove insuline long-acting sono state introdotte, Degludec e Glargine-300. Degludec, il cui nome deriva dall’eliminazione dalla molecola di insulina umana del residuo di treonina acido in posizione B30 (DesB30), dall’aggiunta di acido glutamico (Glu) e dal legame con un acido esadecandiolico (Dec) [22], è un’insulina ultra-lenta, caratterizzata dalla formazione, nel tessuto sottocutaneo, di multi-esameri stabili e solubili, in grado di formare un deposito. La sua emivita è di 24 ore e gli effetti metabolici sono ancora presenti ben oltre le 24 ore dalla somministrazione [23]. Gli studi clinici di fase 3 condotti hanno mostrato un rischio di ipoglicemia globale e di ipoglicemia notturna significativamente inferiore con insulina Degludec rispetto a insulina Glargine-100 (RR 0,83 e 0,68, rispettivamente) [24]. Glargine U300 è una nuova formulazione, più concentrata, di insulina Glargine U100, senza ulteriori differenze molecolari, approvata nel 2015 da FDA. Dopo la somministrazione, Glargine U300 forma un deposito sottocutaneo compatto, che permette un rilascio graduale, prolungato e con profilo di azione ancora più piatto rispetto a Glargine, garantendo un controllo glicemico per circa 36 ore. Anche l’utilizzo di Glargine U300 ha mostrato ridotta incidenza di episodi ipoglicemici notturni e di ipoglicemie gravi rispetto a U100 [25].
Gli analoghi dell’insulina ad azione rapida hanno rappresentato un grande passo in avanti per l’ottimizzazione della glicemia post-prandiale [26], caratterizzati da inizio di azione più rapido e durata di azione più breve rispetto all’insulina umana. I tre analoghi rapidi a oggi più utilizzati (Aspart, Lispro, Glulisine, Tabella 1) possono essere considerati molto simili tra di loro in rapporto all’indicazione terapeutica principale, poiché condividono identico meccanismo di azione, stessa efficacia clinica e stesso profilo di sicurezza (Standard Italiani per la cura del Diabete Mellito 2016).
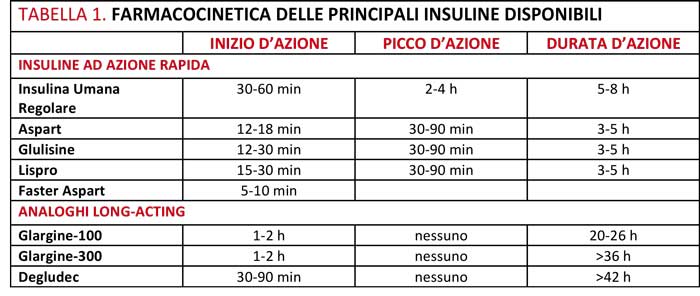
Tuttavia, sebbene gli analoghi dell’insulina rapida abbiano superato in gran parte i limiti dell’insulina umana/regolare, ancora non riproducono pienamente il drastico aumento di insulina circolante che fa seguito all’ingestione di un pasto nei soggetti non diabetici. È stato recentemente approvato dall’UE un nuovo analogo dell’insulina ad azione ultrarapida (Faster Aspart), caratterizzato da un inizio di azione quasi immediato (5 minuti dalla somministrazione), ottenuto grazie all’aggiunta a insulina ricombinante Aspart di un legame con nicotinamide (Vitamina B3) e arginina (stabilizzatore) [27]. Attualmente ancora in fase di sviluppo invece Biochaperone Lispro che ha mostrato risultati positivi in 6 studi clinici [28].
Nuove Tecnologie
Nell’ultimo decennio l’avanzamento dei mezzi informatici e della tecnologia ha permesso di migliorare drasticamente la qualità di vita dei pazienti affetti da T1D. Il trattamento insulinico mediante microinfusore sottocutaneo (Continuous subcutaneous insulin infusion – CSII), oltre a permettere maggiore flessibilità terapeutica, è stato dimostrato essere in grado di ridurre la frequenza degli episodi di ipoglicemia grave e la progressione delle complicanze a lungo termine del diabete, rispetto alla classica terapia insulinica multi-iniettiva [29, 30]. La cosiddetta “sensor-augmented pump (SAP) therapy”, che consiste nel posizionamento di CSII abbinato a monitoraggio in continuo della glicemia interstiziale (continuous glucose monitor – CGM), è considerata a oggi il gold standard terapeutico nel T1D [31] ed è risultata essere in grado non solo di ridurre sia la durata che la gravità degli episodi ipoglicemici, ma, in alcuni casi, addirittura di prevenirli, sulla base dell’andamento glicemico.
Attualmente, sono disponibili in commercio 2 generazioni di SAPs: nella prima il CSII e il CGM operano indipendentemente e il paziente deve integrare correttamente i dati per effettuare aggiustamenti della terapia insulinica; nella seconda, il software di CSII e i valori derivati da monitoraggio CGM sono accoppiati, in modo da permettere sospensioni automatiche del rilascio di insulina in base ai valori predetti di glicemia interstiziale. In entrambi i casi, la gestione della terapia insulinica prandiale è affidata al paziente, preferibilmente supportato dall’utilizzo di un calcolatore di bolo insulinico. Il trial clinico STAR 3 ha mostrato i benefici di SAP-therapy in 329 adulti e 156 bambini, con un follow-up di circa 18 mesi, con una significativamente maggiore riduzione di emoglobina glicata nei pazienti in SAP rispetto ai pazienti in terapia insulinica multi-iniettiva (7,5 vs 8,1 per cento, P < 0,001), senza differenze significative per quanto riguarda il tasso di episodi ipoglicemici [32].
Questi ottimi risultati sono stati resi possibili, negli ultimi anni, soprattutto dall’avanzamento tecnologico dei sistemi di monitoraggio glicemico. Infatti, i sensori glicemici hanno progressivamente migliorato la precisione del dato glicemico ottenuto [33, 34], raggiungendo un’accuratezza approssimativamente del ±10 per cento MARD (mean absolute relative difference). Kovatchev et al. [35] hanno dimostrato che una MARD del 10 per cento è sufficiente a permettere aggiustamenti della posologia insulinica, in assenza di ulteriori controlli di glicemia capillare.
Diversamente dal CGM, i sistemi di Flash glucose monitoring sono oggi considerati un sottogruppo di sistema di monitoraggio glicemico, caratterizzato dall’ottenimento del dato mediante la scansione del sensore mediante un lettore o un telefono cellulare [36]. A differenza dei CGM, i Flash glucose monitoring non forniscono un grafico real-time dell’andamento glicemico, non dispongono di allarmi e non sono utilizzabili per un sistema di monitoraggio integrato con CSII. Possono tuttavia generare grafici retrospettivi dell’andamento glicemico, non necessitano calibrazioni, hanno dimensioni e peso trascurabili e sono generalmente ottimamente accettati dai pazienti diabetici grazie alla loro semplicità d’uso. Infine, data la confermata utilità e sicurezza dei sistemi di CGM, sono da poco disponibili sensori glicemici impiantabili nel sottocute, a lungo termine, della durata di 3 e 6 mesi [37]. In conclusione, lo sviluppo dei sistemi di CGM sta avanzando rapidamente, perfezionando la funzionalità dei sensori, gli algoritmi e i sistemi di integrazione con la pompa insulinica, allo scopo di ottenere un sistema ad ansa chiusa e la creazione del cosiddetto pancreas artificiale.
Trapianti
Per i pazienti che non raggiungono un buon controllo glicometabolico con le nuove terapie e tecnologie, o in cui insorgono a seguito di queste ultime effetti indesiderati che impattano la qualità della vita, un’ulteriore opzione terapeutica è rappresentata dal trapianto di pancreas per ripristinare la produzione di insulina [38]. A causa dei rischi associati alla procedura di trapianto e alla necessità di immunosoppressione per tutta la vita, il trapianto di pancreas è un’opzione terapeutica solo per alcuni pazienti diabetici attentamente selezionati. In base alla funzionalità renale, il trapianto di pancreas può essere infatti effettuato solo in tre categorie di destinatari: pazienti uremici, pazienti post-uremici (a seguito del trapianto di rene con esito positivo) e pazienti non uremici. I pazienti uremici dovrebbero idealmente ricevere un pancreas e un rene in una singola procedura (trapianto simultaneo di rene e pancreas). I pazienti post-uremici con una buona riserva renale potrebbero ricevere un trapianto sequenziale di pancreas (trapianto di pancreas dopo trapianto di rene). I riceventi non uremici possono essere eleggibili per un trapianto di pancreas solitario se hanno uno scarso controllo metabolico nonostante una terapia insulinica ottimale o se soffrono di complicazioni croniche progressive del diabete. Il trapianto di pancreas migliora la qualità della vita dei pazienti con diabete riducendo la progressione delle complicanze croniche e prolungando l’aspettativa di vita dei riceventi [39].
Il trapianto di isole è un’alternativa interessante al trapianto di pancreas per ripristinare la secrezione di insulina in pazienti con T1D. Tuttavia, sebbene sia una procedura meno invasiva, il tasso di successo in termini di indipendenza dall’insulina o secrezione del peptide C è ancora molto inferiore rispetto a quello ottenuto con il trapianto di pancreas intero. Pertanto, anche se il trapianto di isole è una terapia estremamente promettente, attualmente, i risultati ottenuti mantengono come gold stadard il trapianto di pancreas intero [40].
Immunoterapia
Nonostante lo sviluppo di svariati approcci terapeutici per arrestare o ritardare la distruzione delle cellule beta pancreatiche nel T1D autoimmune, il successo rimane vago. Nell’ultimo decennio, abbiamo assistito a un grande aumento delle conoscenze sulla patogenesi del T1D grazie agli studi condotti su topi non obesi diabetici (NOD). Tuttavia, mentre i risultati di questi studi preclinici sembravano essere molto promettenti e incoraggianti, nessuno di questi approcci, una volta testato in contesti clinici, ha portato alla remissione del T1D. La maggior parte degli studi clinici di immunoterapia condotti sui pazienti affetti T1D non ha infatti dimostrato alcun effetto sulla funzione delle cellule beta o sulla richiesta di insulina esogena, sebbene alcuni abbiano raggiunto un ritardo transitorio nella distruzione delle cellule beta con una lieve conservazione del peptide C [41-44].
Dopo la ciclosporina A, il primo agente immunosoppressivo testato, che conservava con successo la funzione beta cellulare, ma che induceva la nefrotossicità e costringeva alla conclusione anticipata dello studio [45, 46], fu introdotta l’idea di indurre tolleranza agli autoantigeni. Tuttavia, l’induzione di questo tipo di tolleranza potrebbe non portare specificamente al blocco delle cellule T e B autoreattive che si infiltrano nelle isole pancreatiche. Quindi, per agire in modo mirato sulle cellule immunitarie presenti nelle isole pancreatiche sono stati testati farmaci specifici rivolti verso le cellule T/B dell’infiltrato [47-49]. Purtroppo, questi approcci hanno portato solo a un successo parziale, senza un reale ripristino della normoglicemia, ma con un rallentamento della perdita di C-peptide [47-49]. La scoperta dell’esistenza di una finestra terapeutica molto stretta prima che si giunga a un punto di non ritorno e che le isole non possano più essere ripristinate a seguito dell’attacco autoimmune ci ha aiutato a modificare il nostro approccio.
Le immunoterapie testate, che si sono rivelate un fallimento, potrebbero portare a risultati soddisfacenti se utilizzate durante questa precisa finestra temporale, quando cioè il T1D è agli esordi. Tuttavia, un aspetto da non sottovalutare è l’eterogeneità della malattia nell’uomo. Non è infatti facile identificare il periodo pre-diabetico in cui inizia lo sviluppo degli autoanticorpi, ma si ha una massa di beta cellule sufficiente e funzionale [50].
Cellule Staminali
Recentemente sono stati riportati i risultati di 4 studi sull’uso di trapianto autologo di cellule staminali ematopoietiche (AHSCT) accompagnato da un regime di condizionamento in pazienti affetti da T1D [51-55]. In tutti questi studi il risultato è stato sorprendente: gli individui trattati con AHSCT hanno mostrato un aumento dei livelli di peptide C, riflettendo un miglioramento nella funzione delle cellule beta pancreatiche, associato a una riduzione di HbA1c che è stata mantenuta fino a 2 anni di follow-up. Alcuni soggetti hanno addirittura raggiunto la remissione completa della patologia per un periodo medio di circa 19 mesi [56].
Inoltre, dopo AHSCT, individui che erano positivi agli autoanticorpi contro gli antigeni delle cellule beta all’inizio dello studio passarono a uno stato negativo per quegli autoanticorpi, con una riduzione dei livelli di citochine pro-infiammatorie (IL-17, IL-1, TNF-α) [56]. Questi studi hanno confermato l’efficacia di una combinazione di cellule staminali e immunosoppressione nell’indurre la remissione di T1D. Tuttavia, questo genere di approccio comporta l’insorgenza di effetti collaterali non indifferenti e per questo si sta tentando di andare verso l’infusione di un numero ridotto di cellule staminali che devono però essere più selezionate. Un approccio promettente per superare questo problema prevede l’isolamento delle cellule staminali dal paziente, il trattamento in vitro di queste cellule per ottenere l’espressione di specifiche proteine coinvolte nell’insorgenza del T1D e la re-infusione delle stesse cellule nello stesso paziente così da bypassare gli eventi avversi associati all’immunosoppressione.
L’obiettivo è quello di ottenere la reversione della patologia grazie all’induzione dell’espressione di specifiche molecole con attività regolatoria nei confronti della risposta autoimmune, come ha dimostrato il gruppo di Paolo Fiorina in un modello preclinico di diabete [57]. In questo studio il trattamento delle cellule staminali isolate è stato effettuato tramite terapia farmacologica o terapia genica così da ripristinare l’espressione della proteina PD-L1 coinvolta nella modulazione della risposta immunitaria, ottenendo la reversione della patologia nel modello preclinico.
Conclusioni
In conclusione, negli ultimi anni la ricerca scientifica ha portato allo sviluppo di approcci terapeutici innovativi promettenti, consentendo di avvicinarsi sempre più allo sviluppo di una cura per il diabete di tipo 1.
BIBLIOGRAFIA
American Diabetes Association. Classification and Diagnosis of Diabetes: Standards of Medical Care in Diabetes-2018. Diabetes Care. 2018; 41(Suppl 1): S13-S27. Epub 2017/12/10. doi: 10.2337/dc18-S002. PubMed PMID: 29222373.
Maahs DM et al. Epidemiology of type 1 diabetes. Endocrinol Metab Clin North Am. 2010; 39(3): 481-97. Epub 2010/08/21. doi: 10.1016/j.ecl.2010.05.011. PubMed PMID: 20723815; PubMed Central PMCID: PMCPMC2925303.
Fiorina P. Beta-Cells step up in controlling the autoimmune response. Diabetes. 2010; 59(8): 1861-4. Epub 2010/07/30. doi: 10.2337/db10-0662. PubMed PMID: 20668291; PubMed Central PMCID: PMCPMC2911052.
Michels AW, Eisenbarth GS. Immunologic endocrine disorders. J Allergy Clin Immunol. 2010; 125(2 Suppl 2): S226-37. Epub 2010/03/05. doi: 10.1016/j.jaci.2009.09.053. PubMed PMID: 20176260; PubMed Central PMCID: PMCPMC2835296.
Cheung N et al. Diabetic retinopathy. Lancet. 2010; 376(9735): 124-36. Epub 2010/06/29. doi: 10.1016/S0140-6736(09)62124-3. PubMed PMID: 20580421.
Diabetes Control and Complications Trial Research Group. Effect of intensive diabetes treatment on the development and progression of long-term complications in adolescents with insulin-dependent diabetes mellitus: Diabetes Control and Complications Trial. J Pediatr. 1994; 125(2): 177-88. Epub 1994/08/01. PubMed PMID: 8040759.
Chaturvedi N et al. Microalbuminuria in type 1 diabetes: rates, risk factors and glycemic threshold. Kidney Int. 2001; 60(1): 219-27. Epub 2001/06/26. doi: 10.1046/j.1523-1755.2001.00789.x. PubMed PMID: 11422754.
Boulton AJ et al. Diabetic neuropathies: a statement by the American Diabetes Association. Diabetes Care. 2005; 28(4): 956-62. Epub 2005/03/29. PubMed PMID: 15793206.
Pop-Busui R et al. Diabetic Neuropathy: A Position Statement by the American Diabetes Association. Diabetes Care. 2017; 40(1): 136-54. Epub 2016/12/22. doi: 10.2337/dc16-2042. PubMed PMID: 27999003.
Melton LJ, 3rd et al. Incidence and prevalence of clinical peripheral vascular disease in a population-based cohort of diabetic patients. Diabetes Care. 1980; 3(6): 650-4. Epub 1980/11/01. PubMed PMID: 7449595.
Rader DJ. Effect of insulin resistance, dyslipidemia, and intra-abdominal adiposity on the development of cardiovascular disease and diabetes mellitus. Am J Med. 2007; 120(3 Suppl 1): S12-8. Epub 2007/02/27. doi: 10.1016/j.amjmed.2007.01.003. PubMed PMID: 17320517.
Laing SP et al. Mortality from heart disease in a cohort of 23,000 patients with insulin-treated diabetes. Diabetologia. 2003; 46(6): 760-5. Epub 2003/05/30. doi: 10.1007/s00125-003-1116-6. PubMed PMID: 12774166.
Kannel WB, McGee DL. Diabetes and cardiovascular disease. The Framingham study. JAMA. 1979; 241(19): 2035-8. Epub 1979/05/11. PubMed PMID: 430798.
Buse JB et al. Primary prevention of cardiovascular diseases in people with diabetes mellitus: a scientific statement from the American Heart Association and the American Diabetes Association. Diabetes Care. 2007; 30(1): 162-72. Epub 2006/12/29. doi: 10.2337/dc07-9917. PubMed PMID: 17192355.
Laing SP et al. Mortality from cerebrovascular disease in a cohort of 23 000 patients with insulin-treated diabetes. Stroke. 2003; 34(2): 418-21. Epub 2003/02/08. PubMed PMID: 12574553.
Al-Rubeaan K et al. Diabetic foot complications and their risk factors from a large retrospective cohort study. PLoS One. 2015; 10(5): e0124446. Epub 2015/05/07. doi: 10.1371/journal.pone.0124446. PubMed PMID: 25946144; PubMed Central PMCID: PMCPMC4422657.
Sargen MR et al. Geographic variation in Medicare spending and mortality for diabetic patients with foot ulcers and amputations. J Diabetes Complications. 2013; 27(2): 128-33. Epub 2012/10/16. doi: 10.1016/j.jdiacomp.2012.09.003. PubMed PMID: 23062327; PubMed Central PMCID: PMCPMC3673572.
Cade WT. Diabetes-related microvascular and macrovascular diseases in the physical therapy setting. Phys Ther. 2008; 88(11): 1322-35. Epub 2008/09/20. doi: 10.2522/ptj.20080008. PubMed PMID: 18801863; PubMed Central PMCID: PMCPMC2579903.
Kahn SE et al. Pathophysiology and treatment of type 2 diabetes: perspectives on the past, present, and future. Lancet. 2014; 383(9922): 1068-83. Epub 2013/12/10. doi: 10.1016/S0140-6736(13)62154-6. PubMed PMID: 24315620; PubMed Central PMCID: PMCPMC4226760.
Rossetti P et al. Superiority of insulin analogues versus human insulin in the treatment of diabetes mellitus. Arch Physiol Biochem. 2008; 114(1): 3-10. Epub 2008/05/10. doi: 10.1080/13813450801900777. PubMed PMID: 18465353.
Shank ML et al. Bedtime insulin/daytime glipizide. Effective therapy for sulfonylurea failures in NIDDM. Diabetes. 1995; 44(2): 165-72. Epub 1995/02/01. PubMed PMID: 7859936.
Jonassen I et al. Design of the novel protraction mechanism of insulin degludec, an ultra-long-acting basal insulin. Pharm Res. 2012; 29(8): 2104-14. Epub 2012/04/10. doi: 10.1007/s11095-012-0739-z. PubMed PMID: 22485010; PubMed Central PMCID: PMCPMC3399081.



