Nel panorama delle statine un trattamento efficace di primo livello che favorisce sicurezza e tollerabilità
Tra le diverse statine attualmente disponibili esiste una ben definita scala di potenza ipolipemizzante. Il clinico ha quindi a disposizione diverse opzioni per calibrare la terapia sulle specifiche condizioni cliniche dei pazienti, tenendo conto del rischio di effetti collaterali, soprattutto nella popolazione anziana con pluripatologie.
Le linee guida ESC/EAS pubblicate alla fine del 2019 [1] hanno riaffermato l’importanza della riduzione della colesterolemia come pietra angolare della prevenzione primaria e secondaria delle malattie cardiovascolari aterosclerotiche. E lo hanno fatto consolidando una tendenza in atto da alcuni anni, cioè rendendo ancora più stringenti le raccomandazioni d’intervento, secondo il principio the lower, the better, alla luce degli studi che hanno dimostrato i vantaggi clinici di tale approccio e delle prove di efficacia e sicurezza dei trattamenti ipolipemizzanti.
Tuttavia, il clinico che oggi voglia accogliere queste nuove indicazioni emerse dalla evidence based-medicine, deve anche tenere conto che la terapia dev’essere personalizzata. Di conseguenza, la prescrizione di statine, indiscusse protagoniste dell’approccio farmacologico all’ipercolesterolemia, va valutata alla ben nota scala di potenza delle diverse molecole. Particolare attenzione va posta nel trattamento dei pazienti anziani, spesso affetti da pluripatologie, in cui il raggiungimento dei target lipidici ematici dev’essere attentamente bilanciato dalle considerazioni riguardanti la sicurezza. In altre parole, le statine dovrebbero certamente essere prescritte in questa popolazione di soggetti per evitare un evento cardiovascolare, ma con la necessaria cautela, dato che potrebbero presentare effetti collaterali con maggiore frequenza rispetto ai soggetti più giovani [2].
Lo stesso si può dire dei soggetti che hanno un’ipercolesterolemia non grave, e che non necessitano di statine di elevata potenza: occorre considerare che, secondo una stima epidemiologica di alcuni anni fa, poco più di un terzo degli uomini e un terzo circa delle donne si trovano in una condizione border-line, cioè con colesterolemia compresa tra 200 e 239 mg/dL [3].
In tutti questi casi, può essere vantaggioso ricorrere a una statina di primo livello, con un profilo favorevole di efficacia e sicurezza come lovastatina. Questa molecola ha rappresentato il primo inibitore della HMG-CoA reduttasi a essere introdotto nella terapia, circa 35 anni fa, ed è quindi molto ben conosciuta in tutti i suoi aspetti (per un approfondimento sui risultati di efficacia e sicurezza di lovastatina, si rimanda ai prossimi paragrafi).
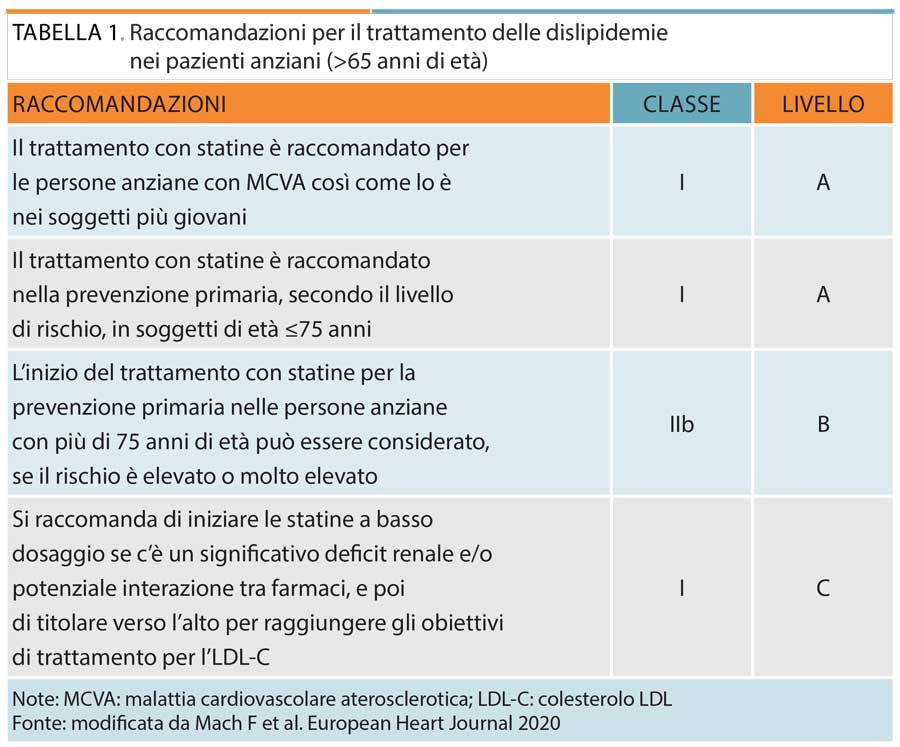
L’importanza del ruolo di lovastatina in particolari popolazioni di pazienti è ribadito dalle ultime linee guida ESC/EAS per il trattamento dell’ipercolesterolemia in soggetti ultrasessantacinquenni (Tabella 1) così come dalla recente Nota 13 dell’Agenzia italiana del farmaco (AIFA) [4] che recepisce tali indicazioni. Da rilevare come ai fini della rimborsabilità, i pazienti anziani con pluripatologie vengano considerati a tutti gli effetti in prevenzione secondaria.
Efficacia di lovastatina: i risultati degli studi
Il profilo di efficacia di lovastatina è stato valutato in diversi studi. I principali per ampiezza delle popolazioni coinvolte e per rilevanza dei risultati, sono i trial denominati, rispettivamente, EXCEL, AFCAPS/TexCAPS, CCAIT.
Lo studio EXCEL
Il trial denominato Expanded Clinical Evaluation of Lovastatin (EXCEL) [5] è uno studio multicentrico, in doppio cieco, controllato rispetto alla dieta e rispetto al placebo in 8.245 soggetti con ipercolesterolemia. I pazienti sono stati randomizzati a ricevere lovastatina alla dose di 20 mg/die, 40 mg/die, 20 mg/bid o 40 mg/bid per 48 settimane.
Dall’analisi statistica dei dati è emerso che l’assunzione di lovastatina ha prodotto cambiamenti sostenuti e dose-correlati nel profilo lipidico dei soggetti arruolati (Figura 1).
Figura 1. Efficacia di lovastatina sulle componenti LDL e HDL del colesterolo,
colesterolo totale e trigliceridi
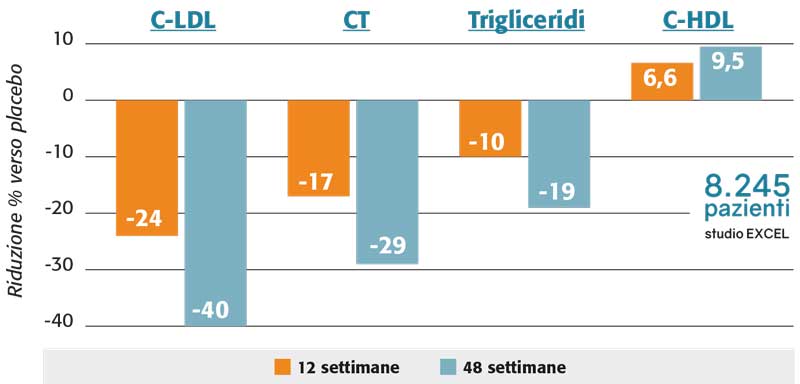
Note: CT, colesterolo totale; C-HDL, colesterolo HDL; C-LDL, colesterolo LDL.
Fonte: modificata da Bradford FH et al. Arch Intern Med 1991
L’obiettivo di un livello di colesterolo LDL inferiore a 4,14 mmol/L (160 mg/dL) è stato raggiunto dall’80 per cento (%) al 96% dei pazienti, mentre l’obiettivo di un livello di colesterolo inferiore a 3,36 mmol/L (130 mg/dL) è stato raggiunto dal 38% all’83% dei pazienti. Per quanto riguarda la sicurezza, la differenza tra lovastatina e placebo nell’incidenza di eventi clinici avversi che hanno richiesto l’interruzione è stata piccola, e andava dall’1,2% per il dosaggio di 20 mg/bid all’1,9% per il dosaggio di 80 mg/die. Più nello specifico, incrementi del livello di transaminasi superiori a tre volte il limite superiore della norma sono stati osservati:
- nello 0,1% dei pazienti che hanno assunto placebo e 20 mg/die di lovastatina,
- nello 0,9% di coloro che hanno ricevuto 40 mg/die di lovastatina,
- nell’1,5% dei soggetti che hanno assunto 80 mg/die di lovastatina.
La miopatia, definita come sintomi muscolari con un’elevazione della creatina chinasi superiore a 10 volte il limite superiore della norma, è stata riscontrata in un solo paziente (0,1%) che ha ricevuto 40 mg/die di lovastatina e quattro pazienti (0,2%) che hanno ricevuto 80 mg/die.
Secondo le conclusioni degli Autori, i risultati dello studio dimostrano che lovastatina, se aggiunta dopo una sperimentazione adeguata di una dieta a basso contenuto di lipidi, è un trattamento altamente efficace e generalmente ben tollerato per i pazienti con ipercolesterolemia moderata.
Lo studio AFCAPS/TexCAPS
Uno studio successivo a EXCEL, condotto in Texas e denominato AFCAPS/TexCAPS [6], ha verificato l’efficacia di lovastatina nel prevenire gli eventi cardiovascolari in soggetti senza malattia coronarica clinicamente evidente e con valori di colesterolo totale e LDL nella media (o moderatamente elevati) e con livelli di colesterolo HDL inferiori alla media. Si tratta di uno studio, randomizzato, in doppio cieco, controllato con placebo in cui sono stati arruolati 5.608 uomini e 997 donne. I pazienti sono stati randomizzati a ricevere lovastatina (20-40 mg) o un placebo in aggiunta a una dieta a basso contenuto di grassi saturi e basso contenuto di colesterolo. Alla fine del periodo di studio, i ricercatori hanno verificato il manifestarsi di un primo evento coronarico acuto maggiore definito come infarto miocardico fatale o non fatale, angina instabile o morte cardiaca improvvisa (Figura 2).
Figura 2. Riduzione del rischio cardiovascolare (studio AFCAPS/TexCAPS)
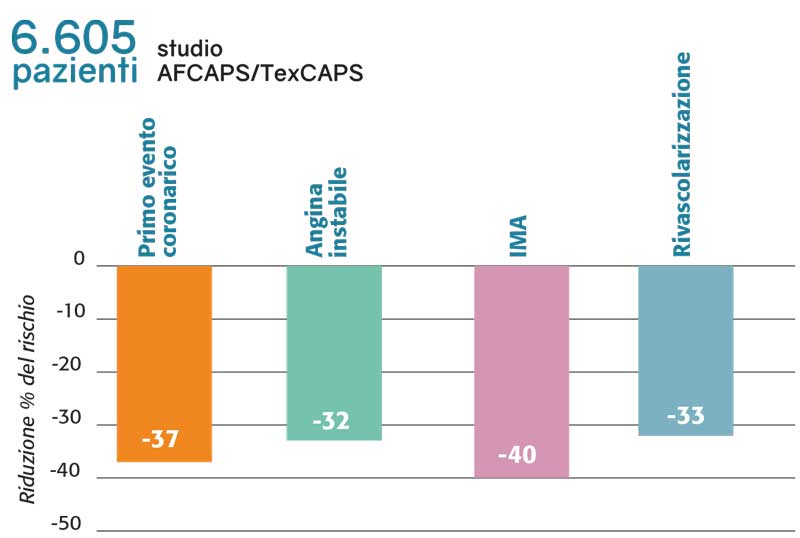
Note: IMA, infarto miocardico acuto.
Fonte: modificata da Downs JR et al. Jama 1998
Dopo un follow-up medio di 5,2 anni, la lovastatina (20-40 mg al giorno) ha ridotto le LDL-C del 25% a 2,96 mmol/L (115 mg/dL) e ha aumentato le HDL-C del 6% a 1,02 mmol/L (39 mg/dL).
Infine, non sono emerse differenze clinicamente rilevanti nei parametri di sicurezza tra i gruppi di trattamento.
Secondo le conclusioni degli Autori, dunque lovastatina riduce il rischio di un evento coronarico acuto in donne e uomini con valori di colesterolo totale e colesterolo LDL nella media (o moderatamente elevati) e colesterolo HDL sotto la media, supportando l’inclusione del colesterolo HDL tra i fattori di rischio e confermando i benefici della riduzione del colesterolo LDL.
Lo studio CCAIT
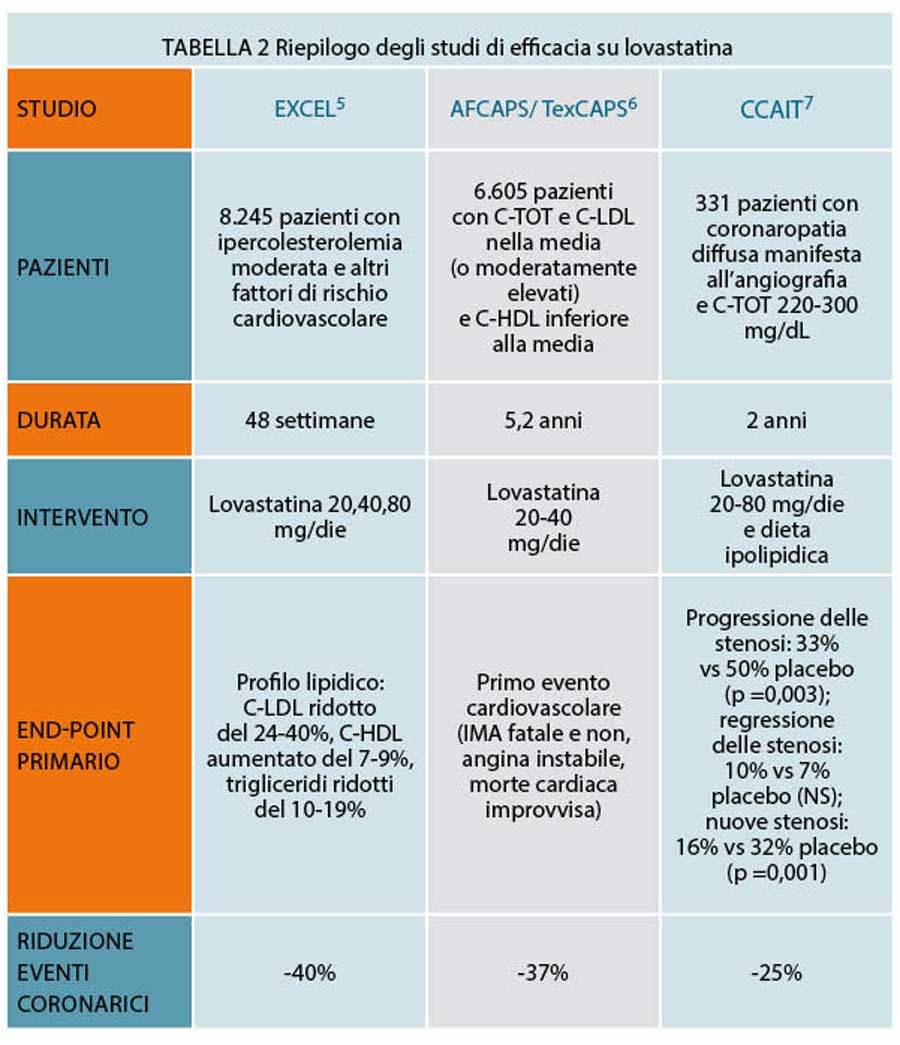
I risultati dello studio AFCAPS/TexCAPS vengono sostanzialmente confermati da un altro trial denominato CCAIT [7] che ha indagato gli effetti sulla salute cardiovascolare della monoterapia con lovastatina. In questo studio randomizzato, in doppio cieco, controllato con placebo, sono stati arruolati 331 pazienti con aterosclerosi coronarica diffusa ma non necessariamente grave, documentata da un recente arteriogramma, e con colesterolo ematico a digiuno tra 220 e 300 mg/dL. I soggetti coinvolti hanno ricevuto una consulenza dietetica intensiva e sono stati randomizzati a ricevere lovastatina o placebo alla dose iniziale di 20 mg/die, dose che successivamente è stata titolata a 40 e 80 mg durante le prime 16 settimane, fino a ottenere un livello di colesterolo LDL a digiuno inferiore o uguale a 130 mg/dL. La dose media di lovastatina era di 36 mg/die. L’arteriografia coronarica è stata ripetuta dopo due anni e in 299 pazienti (90%), 3.858 segmenti coronarici con 2.309 stenosi sono stati misurati in cieco con un sistema quantitativo automatizzato e computerizzato. Il colesterolo totale e il colesterolo LDL sono diminuiti del 21+/-11% e del 29+/-11%, rispettivamente, nel braccio di trattamento con lovastatina, mentre sono cambiati per meno del 2% nei pazienti trattati con placebo. L’endpoint primario, il punteggio del cambiamento coronarico, definito come la media per paziente delle variazioni minime del diametro del lume per tutte le lesioni misurate, è peggiorato di 0,09+/-0,16 mm nel gruppo trattato con placebo e di 0,05+/-0,13 mm nel gruppo trattato con lovastatina. Una progressione (un peggioramento del diametro minimo di uno o più stenosi di ≥0,4 mm) senza regressione in altri siti si è verificato in 48 dei 146 pazienti con lovastatina e 76 dei 153 placebo (33% contro il 50%). Nuove lesioni coronariche si sono sviluppate in 23 pazienti con lovastatina e 49 pazienti con placebo. L’effetto benefico del trattamento è risultato più marcato nelle lesioni più numerose e lievi e nei pazienti i cui livelli di colesterolo totale al basale o colesterolo LDL erano superiori alla mediana del gruppo. In tabella 2 sono riassunti gli studi di efficacia su lovastatina.
Sicurezza e tollerabilità
Il controllo del profilo lipidico è dunque riconosciuto da anni come un fattore determinante per la riduzione del rischio cardiovascolare, e le statine hanno un ruolo consolidato nell’approccio farmacologico all’ipercolesterolemia. Negli anni passati tuttavia su questa categoria di farmaci si è concentrata l’attenzione di molti clinici per il verificarsi di alcuni eventi avversi, che hanno avuto un significativo impatto soprattutto sull’aderenza alla terapia da parte dei pazienti. Il rischio correlato a eventi avversi di tipo muscolo-tendineo, insorgenza di diabete e di insufficienza renale acuta sono stati indagati in tre diversi studi, illustrati di seguito in dettaglio.
Eventi avversi muscolo-tendinei
In uno studio del 2012 [8], un gruppo di ricercatori dell’Università della California a San Diego ha analizzato i dati riguardanti gli eventi avversi correlati all’assunzione di statine nell’ampio database AERS della Food and Drug Administration (FDA), focalizzando l’attenzione in particolare sui problemi muscolari.
A questo scopo hanno selezionato alcune molecole: atorvastatina, simvastatina, lovastatina, pravastatina, rosuvastatina e fluvastatina, oltre agli equivalenti generici di ciascuna.
Dall’analisi dei dati è emerso che lovastatina è insieme a pravastatina, la molecola gravata dal minor tasso di rischio per eventi avversi di tipo muscolare (Figura 3).
Figura 3. Profilo di sicurezza muscolo-tendinea: diverse statine a confronto
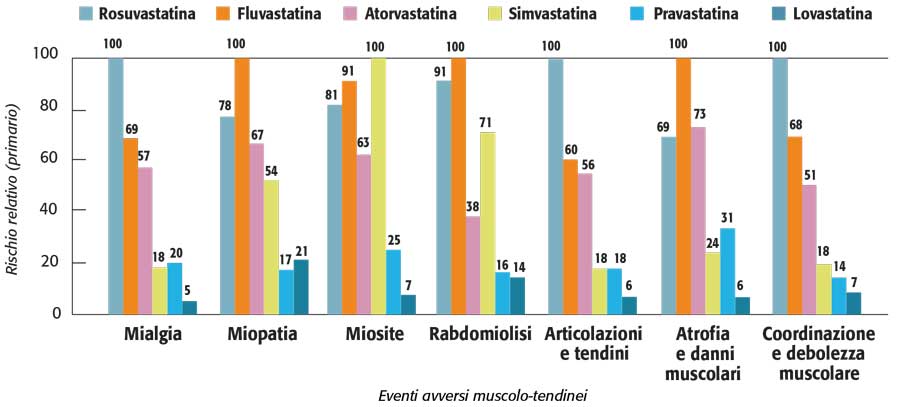
Fonte: modificata da Hoffman KB. PLoS One 2012
Dallo studio è emerso in sostanza che le statine considerate differiscono enormemente tra loro in termini di rischio di eventi avversi muscolo-tendinei e che la potenza relativa della statina è un predittore fondamentale per tale rischio (Figura 3). Questi dati, concludono gli Autori, offrono un importante punto di riferimento per i clinici che devono scegliere la statina da prescrivere ai propri pazienti per la gestione dell’ipercolesterolemia, soprattutto per riprendere la terapia in quei soggetti che hanno già patito questo tipo di eventi avversi.
Rischio di insorgenza di diabete
Lo stesso tipo di correlazione tra potenza delle statine e tasso di eventi avversi è stato riscontrato in uno studio retrospettivo di popolazione condotto in Canada tra il 1997 e il 2010 su pazienti di età maggiore di 65 anni [9]. Gli Autori hanno analizzato i dati di un ampio database di prescrizioni farmacologiche della regione dell’Ontario, considerando soggetti con prima prescrizione di statine dopo il compimento del 66-esimo anno di età ed escludendo i soggetti con diagnosi di diabete prima dell’inizio dello studio.
I dati hanno mostrato che rispetto a pravastatina, il farmaco di riferimento in tutte le analisi, alcune statine erano associate a un incremento del rischio incidente di diabete, con valori di hazard ratio aggiustato di 1,22 per atorvastatina, 1,18 per rosuvastatina, 1,10 per simvastatina. Lovastatina è risultata invece associata con una diminuzione di tale rischio, con un hazard ratio aggiustato di 0,99, così come fluvastatina (0,95).
Rischio d’insufficienza renale
In uno studio pubblicato nel 2013 [10] Colin Dormuth, dell’Università della British Columbia a Vancouver, in Canada, e colleghi hanno stimato il tasso di insufficienza renale in correlazione all’assunzione di statine di differente potenza. A questo scopo hanno condotto uno studio retrospettivo, osservazionale, considerando alcuni database amministrativi, e usando nove studi di coorte e metanalisi, per complessivi 2.067.639 pazienti di età superiore a 40 anni, che hanno iniziato il trattamento con statine tra il 1° gennaio 1997 e il 30 aprile 2008. Ogni soggetto ricoverato per insufficienza renale acuta è stato abbinato a 10 soggetti di controllo.
Gli Autori hanno suddiviso i partecipanti in diversi gruppi in base alla potenza della statina assunta, considerando come trattamenti con statina ad alta potenza i seguenti dosaggi: ≥10 mg rosuvastatina; ≥ 20 mg atorvastatina e ≥40 mg di simvastatina, mentre tutti gli altri trattamenti sono stati considerati a bassa potenza.
Entro 120 giorni di trattamento, si sono verificati 4.691 ricoveri per insufficienza renale acuta in pazienti senza insufficienza renale cronica e 1.896 ricoveri con insufficienza renale cronica. Nei pazienti con malattia renale non cronica, gli attuali utilizzatori di statine ad alta potenza avevano il 34% di probabilità in più di essere ricoverati in ospedale con lesione renale acuta entro 120 giorni dall’inizio del trattamento. Gli utenti di statine ad alta potenza con malattia renale cronica, invece, hanno avuto un aumento del tasso di ricovero solo del 10%.
Secondo le conclusioni degli Autori, l’uso di statine ad alta potenza è associato a un aumento del tasso di diagnosi di lesioni renali acute nei ricoveri ospedalieri rispetto alle statine a bassa potenza. L’effetto sembra essere più forte nei primi 120 giorni dopo l’inizio del trattamento.
Lo stesso tipo di effetto sugli eventi renali acuti in dipendenza dalla potenza delle statine assunte è emerso nello studio di Yu-Heng Chung e colleghi [11] condotto su cartelle cliniche di assicurazioni sanitarie di Taiwan e pubblicato nel 2013. Si tratta di uno studio di coorte su pazienti che hanno iniziato ad assumere statine di elevata potenza ipocolesterolemizzante (atorvastatina e rosuvastatina) e bassa potenza (lovastatina, simvastatina, pravastatina e fluvastatina) tra il 1° gennaio 2001 e il 31 dicembre 2008.
L’outcome di interesse è stato l’insufficienza renale grave, definita come l’endpoint composito di emodialisi, dialisi peritoneale e trapianto di rene. È stato applicato un modello di regressione proporzionale del rischio per stimare il rapporto di incidenza tra i due gruppi, corretto per propensity score in base alle caratteristiche di base. Complessivamente, sono stati raccolti i dati di 26.007 soggetti che hanno iniziato ad assumere statine di elevata potenza e 42.249 soggetti che hanno iniziato ad assumere statine di bassa potenza. Dall’analisi delle cartelle cliniche, è emerso che il tasso di incidenza grezzo per lo sviluppo di insufficienza renale grave è stato, rispettivamente, di 0,65 e 0,46 per 100 anni-persona per i due gruppi. Mentre i due gruppi avevano un rischio comparabile per l’infarto del miocardio, è risultato un aumento del 13% nel rischio di sviluppare un’insufficienza renale grave in chi ha iniziato la terapia con rosuvastatina e atorvastatina. Inoltre, l’aumento del rischio associato a queste due statine è stato coerente tra i diversi gruppi a rischio (diabete, malattie renali croniche e cardiopatie ischemiche).
Gli Autori dunque concludono che le statine con un’elevata efficacia ipocolesterolemizzante potrebbero aumentare il rischio di sviluppare una grave insufficienza renale.
Bibliografia
- Mach F, Baigent C, Catapano AL. 2019 ESC/EAS Guidelines for themanagement of dyslipidaemias: lipid modification to reduce cardiovascular risk. European Heart Journal (2020) 41, 111-188
- Casula M, Catapano Al. La prescrizione delle statine nei pazienti anziani. Care 2019 n 4:22-23
- Pradelli L, Zaniolo O. Il valore clinico ed economico della lovastatina nella prevenzione cardiovascolare primaria. Farmeconomia e percorsi terapeutici 2006; 7(3)
- AIFA. Nota 13
- Bradford RH, Shear CL, Chremos AN et al. Expanded Clinical Evaluation of Lovastatin (EXCEL) Study Results. I. Efficacy in Modifying Plasma Lipoproteins and Adverse Event Profile in 8245 Patients With Moderate Hypercholesterolemia 1991. Arch Intern Med; 151(1):43-9
- Downs JR, Clearfiled M, Whithney E, et al. Primary Prevention of Acute Coronary Events With Lovastatin in Men and Women With Average Cholesterol Levels: Results of AFCAPS/TexCAPS. Air Force/Texas Coronary Atherosclerosis Prevention Study. JAMA 1998; 279(20):1615-22
- Waters D, Higginson L, Gladstone P et al. Effects of Monotherapy With an HMG-CoA Reductase Inhibitor on the Progression of Coronary Atherosclerosis as Assessed by Serial Quantitative Arteriography. The Canadian Coronary Atherosclerosis Intervention Trial. Circulation. 1994 Mar;89(3):959-68
- Hoffman KB, Kraus C, Dimbil M, Golomb BA. A Survey of the FDA’s AERS Database Regarding Muscle and Tendon Adverse Events Linked to the Statin Drug Class. PLOS ONE 2012; 8:e42866
- Carter AA, Gomes T, Mamdani MM. Risk of incident diabetes among patients treated with statins: population based study. BMJ 2013; 346: f2610
- Dormuth CR, Hemmelgarn BR, Paterson JM et al. Use of high potency statins and rates of admission for acute kidney injury: multicenter, retrospective observational analysis of administrative databases. BMJ 2013;346:f880
- Yu-Heng C, Lee YC, Chang CH et al. Statins of High Versus Low Cholesterol-Lowering Efficacy and the Development of Severe Renal Failure Pharmacoepidemiol Drug Saf 2013; 22(6):583-92.



